请注意,本文编写于 1337 天前,最后修改于 353 天前,其中某些信息可能已经过时。
https://i.loli.net/2020/09/05/Wg2UPw7uO51A3Dy.png
你听说过超临界水吗?
作为一个常识,每个人都知道水的沸点会随着气压的升高而升高。在标准大气压下,水的沸点为100℃;在高原地区,大气压力小于标准大气压,水的沸点降低,不足100℃便沸腾,这也是为什么高原地区煮饭需要高压锅这样密闭的容器。那么一直增大压力沸点是不是会一直升高?这里水指液态水。
首先了解一下水的相图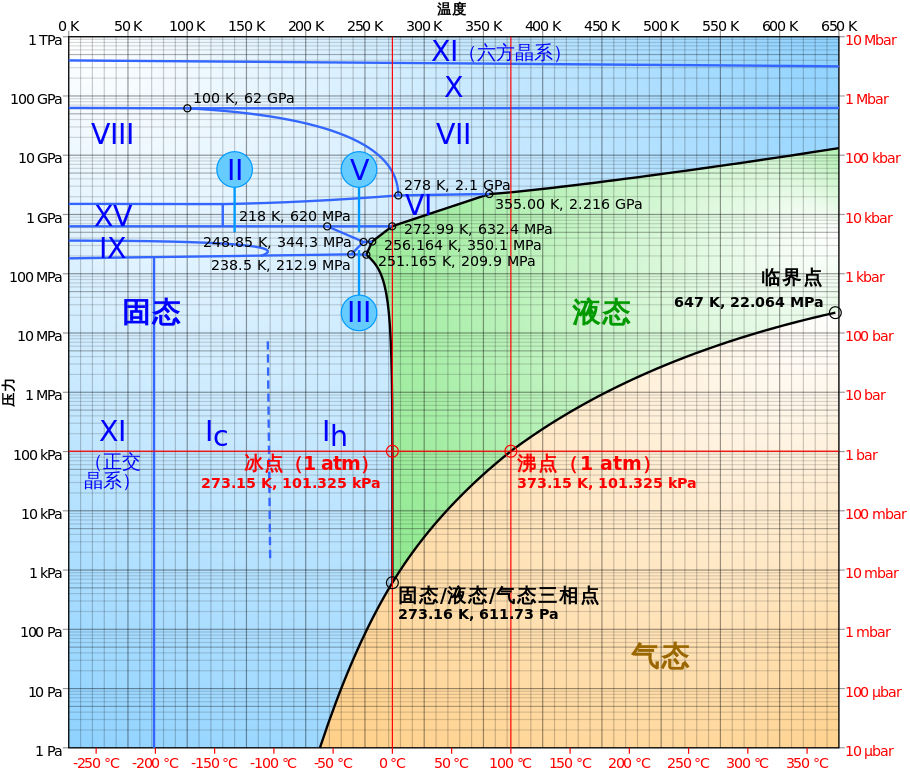
图中纵坐标为压强,绿色和棕色区域相交部分即为水的沸点。在液态水区域,随着压强的升高,水的沸点一直升高。图中绿色的部分即为水的液态区域,其右侧有一临界点,标注着647K,即374℃,表明液态水的最高温度为374℃,并非想象中的没有上限。此时的临界压强为22.064MPa,超过这个压强,水的沸点将不复存在,也就是说,继续加热并不会导致水沸腾。
当温度超过临界温度374℃,水会进入超临界状态。此时水处于气液不分的状态,没有明显的气液分界面,既不是液体也不是气体。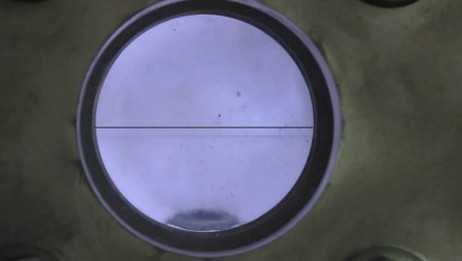
在理想情况下,一个密闭刚体容器,里面装有足够量的水,给容器不断加热。在这个过程中,容器内的温度和压强不断上升。在低压阶段,可以明显看到液态和气态两种状态存在,且分界面明显。水接近亚临界状态时,分界面渐渐模糊,在达到临界点瞬间,分界面消失,水进入超临界状态。
超临界水和普通的水有什么区别?
物理性质:超临界水的密度比普通的水小;
化学性质:1.超临界水溶解性更强;2.在超临界水中的化学反应速度更快;3.注入氧气后具有极强的氧化性。